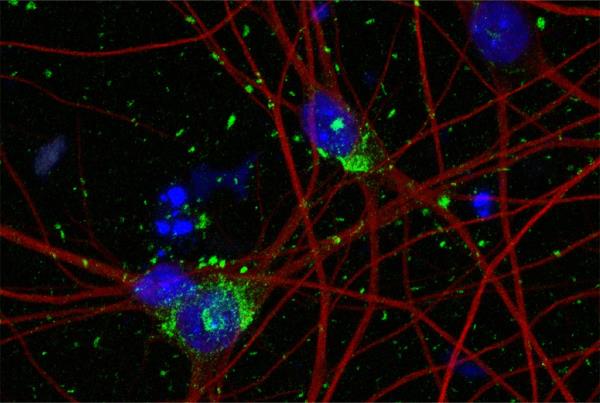
人类干细胞来源的神经元染色显示细胞核(蓝色)、神经元细胞骨架(红色)和tau聚集物(绿色)中的DNA。来源:Jesus Madero Perez
威尔康奈尔医学院的科学家们开发了一种创新的人类神经元模型,该模型有力地模拟了tau蛋白聚集体在大脑中的扩散——这一过程导致了阿尔茨海默病和额颞叶痴呆的认知能力下降。这个新模型已经导致了可能潜在地阻止tau扩散的新治疗靶点的鉴定。
这项临床前研究发表在4月5日的《细胞》杂志上,是阿尔茨海默病研究的重大进展。
该研究的主要作者、海伦和罗伯特·阿佩尔阿尔茨海默病研究所所长、威尔康奈尔医学院菲尔家族大脑和精神研究所神经退行性疾病伯顿·p和朱迪思·b·雷斯尼克杰出教授李干博士说:“目前没有任何治疗方法可以阻止tau聚集物在阿尔茨海默病患者大脑中的扩散。”“我们的tau病毒传播的人类神经元模型克服了以前模型的局限性,并揭示了以前未知的药物开发的潜在目标。”
人类多能干细胞可以发育成身体的任何细胞,并且可以在实验室培养皿中被诱导成神经元来模拟脑部疾病。然而,在这些年轻神经元中建立tau蛋白繁殖模型几乎是不可能的,因为tau蛋白在衰老的大脑中繁殖需要几十年的时间。
Tau扩散模型的研究进展
甘博士的团队使用CRISPR技术修改了人类干细胞的基因组,促使它们表达与患病的衰老大脑相关的tau蛋白。甘博士说:“这个模型改变了游戏规则,可以在几周内模拟tau蛋白在神经元中的扩散,而在人脑中,这一过程通常需要几十年。”
在寻求阻止tau蛋白传播的过程中,甘博士的团队采用CRISPRi筛选方法禁用了1000个基因,以确定它们在tau蛋白传播中的作用。他们发现了500个对tau蛋白丰度有重大影响的基因。
该研究的主要作者之一Celeste Parra Bravo说:“CRISPRi技术使我们能够使用无偏见的方法来寻找药物靶点,而不局限于其他科学家之前报道的内容。”Celeste Parra Bravo是威尔康奈尔医学科学研究生院在Gan实验室工作的神经科学博士候选人。
对治疗的发现和启示
其中一项发现包括ufmyation级联,这是一个细胞过程,涉及一种名为UFM1的小蛋白质附着在其他蛋白质上。这一过程与tau蛋白扩散的关系此前是未知的。对阿尔茨海默病患者大脑的尸检研究发现,ufmyation发生了改变,研究小组还在临床前模型中发现,抑制ufmyation所需的酶可以阻断tau在神经元中的繁殖。
“我们特别受鼓舞的是,证实抑制ufmyation阻断了tau在人类神经元和小鼠模型中的传播,”该论文的合著者、威尔康奈尔医学院阿佩尔研究所神经科学研究副教授龚晓青博士说。
甘博士说,许多阿尔茨海默病的治疗方法最初在小鼠模型中显示出希望,但在临床试验中没有成功。有了新的人类细胞模型,她对未来的道路持乐观态度。“我们在人类神经元中的发现为开发新的治疗方法打开了大门,这些治疗方法可以真正改变那些患有这种毁灭性疾病的人。”
参考:作者:Celeste Parra Bravo、Alice Maria Giani、Jesus Madero Perez、Zeping Zhao、Yuansong Wan、Avi J. Samelson、Man Ying Wong、Alessandro Evangelisti、Ethan Cordes、Li Fan、peararly Ye、Daphne Zhu、Tatyana Pozner、Maria Mercedes、Tark Patel、Allan Yarahmady、Gillian K. Carling、Fredrik H. Sterky、Virginia M.Y. Lee、Edward B. Lee、Michael DeTure、Dennis W. Dickson、Manu Sharma、Sue-Ann Mok、Wenjie Luo、mingui Zhao、Martin Kampmann、龚晓卿、甘丽,2024年4月5日,《细胞》。DOI: 10.1016 / j.cell.2024.03.015
为您推荐:
- 伊朗在亚洲杯点球大战中获胜,叙利亚心碎 2025-07-22
- 麦当劳的厨师透露了菜单上著名菜品的配方 2025-07-22
- 为了防止绣球花在冬天死亡,你现在需要做四个绝对重要的任务 2025-07-22
- 风暴“巴贝特”带来的250毫米降雨预计将引发严重洪灾,并发出红色预警 2025-07-22
- 亚马逊购物者喜欢“方便”的迷你雨伞,可以“突然下雨”,售价仅为8英镑 2025-07-22
- 以色列应对哈马斯的方式应该是维持与沙特的协议 2025-07-22


